近日,大连化物所蛋白质折叠化学生物学创新特区研究组(02T5组)刘宇研究员团队、生物分子高效分离与表征研究组(1810组)张丽华研究员团队,以及西湖大学张鑫教授团队等合作,通过系统性调控绿色荧光蛋白发色团的骨架结构,实现分子的三重态化学活性,并用于活细胞内聚集态蛋白质的靶向交联,获得了聚集态蛋白质的相互作用信息。 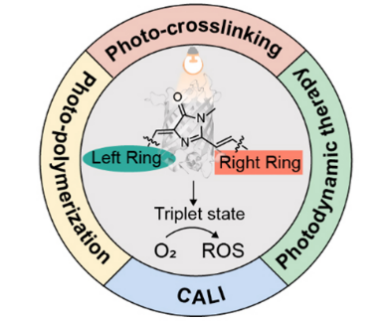
蛋白质的错误折叠、变性与聚集会引发多种蛋白质构型疾病,如阿尔兹海默症、帕金森症、渐冻人症和淀粉样心肌病等。目前,聚集态蛋白的研究主要停留在发展荧光探针观察其位置形貌并示踪聚集过程,用于疾病的早期发现和临床诊断。然而,用于解析细胞内聚集态的蛋白质组成成分和相互作用信息的分析工具鲜有报道。聚集态蛋白质的组分和互作信息对于揭示上述疾病的发病机制,寻找新的诊疗靶点具有积极的科学和临床意义。 近年来,刘宇团队针对细胞内聚集态蛋白质缺乏完整三维结构信息、难以实现靶向探测这一领域难点,提出靶向聚集态蛋白质内部孔道特征微环境的探针设计思路(Angew. Chem. Int. Ed.,2021;Angew. Chem. Int. Ed.,2021),实现了胞内致病聚集态蛋白的位置形貌分析(Anal. Chem.,2021)、共聚集过程的机制解析(Chem. Sci.,2021)和内部微环境异质性的定量分析(Angew. Chem. Int. Ed.,2021;ACS Sens.,2022)。然而,上述工作仅局限于蛋白质聚集过程的动态观测,缺乏对其组成成分和相互作用的进一步剖析。 本工作中,刘宇团队与张丽华团队合作,通过衍生天然荧光蛋白的发色基团,实现其三重态光交联性质的理性调控,并利用该分子骨架结构对聚集态蛋白质的胞内靶向结合,实现对聚集态蛋白的组分和互作信息的规模化解析。此外,刘宇团队和张鑫团队利用绿色荧光蛋白发色团骨架(HBI),进行分子结构衍生并实现了规律性调控分子产生活性氧的效率,为蛋白质的化学邻近标记奠定基础。针对标记蛋白的高度复杂性、难鉴定的挑战,张丽华团队通过发展高精准、高通量的蛋白质相互作用解析技术,对光氧化和光交联聚集态蛋白质光反应类型和修饰位点进行了高灵敏度鉴定,进而实现了聚集态蛋白质的组分和互作信息的高可信度确认。同时,我所吴凯丰研究员团队和华盛顿大学李晓松教授团队通过分子激发态测量和理论计算,探讨了该类分子三重态化学的机制,为本工作的光氧化和光交联提供了理论支撑。作为一类仿生新型的光敏剂和光交联剂,该工作也展示了其在发色团辅助光失活(CALI),光动力治疗(PDT),以及有机光聚合反应等场景的应用潜力。 上述成果以“Enabling Photo-Crosslinking and Photo-Sensitizing Properties for Synthetic Fluorescent Protein Chromophores”为题,于近日发表在《德国应用化学》(Angew. Chem. Int. Ed.)上。该工作的第一作者是大连化物所02T5组博士研究生冯焕和1810组赵群研究员(第十批会员)。该工作得到了国家自然科学基金、国家重点研发计划、中国科学院青年创新促进会、美国国家科学基金等项目的资助。(文/图 冯焕、赵群) 文章链接
| 